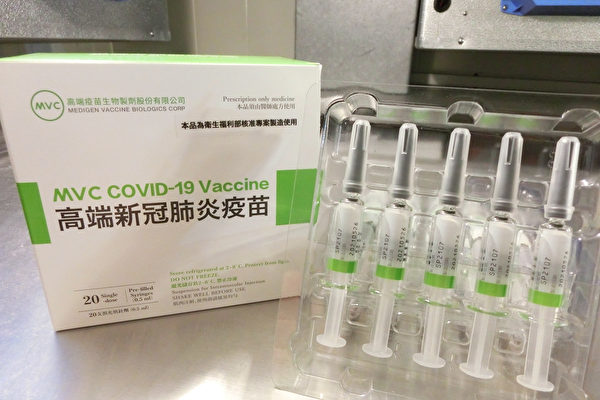
【大纪元2021年08月02日讯】(大纪元记者赖玟茹台湾台北报导)食药署昨(2)日公布高端疫苗紧急授权(EUA)的专家审查会议纪录,多数与会专家同意高端通过紧急使用授权,但不少专家都针对“T细胞免疫反应”提出意见,希望高端补足有关T细胞相关反应的数据,并对Delta变异株的保护力仍存有疑虑。
本次会议出席专家共21人,除主席不参与投票外,通过3人、有条件通过15人、补件再议1人、不通过1人。
多数与会专家同意高端通过紧急使用授权,但不少专家都针对“T细胞免疫反应”提出意见,希望高端补足有关T细胞相关反应的数据。
另外,也有多位专家关注对病毒变异株的保护力。有专家表示,疫苗对部分病毒变异株所产生中和抗体效价有降低情形,对Delta变异株的保护力仍有疑虑,但中和抗体效价高低能否作为疫苗保护力指标,以现有数据恐不足以支持,有待厂商后续提供更多免疫原性及疫苗保护力资料来厘清。
除高端疫苗对印度Delta变种病毒保护力受专家质疑外,根据美国疾病管制暨预防中心(CDC)最新的研究发现,占比高达8成9打完疫苗后,仍感染Delta变种病毒,其中有7成4的民众已打完两剂疫苗,其接种的疫苗厂牌,辉瑞BNT疫苗(占46%)、莫德纳(38%),及仅需注射单剂的娇生(16%)。
国产疫苗为何能提前量产?陈时中:为加速研发
26万多剂高端疫苗2日完成检验封缄,回推时间后发现,早在紧急授权(EUA)通过前就已经量产,引发外界质疑。指挥中心指挥官陈时中解释,为加速疫苗研发,各国采取不同方式简化行政流程,若等EUA通过才量产送验,恐怕得多等3个月至半年才有疫苗可以接种。
高端研发的疫苗于7月19日通过紧急使用授权(EUA),首4批26万5,528剂高端疫苗却在8月2日就完成检验并核发封缄证明书,也就是说,高端在取得EUA前半个月就已将疫苗送验。
对于国产疫苗为何能够提前量产?陈时中说明,一般检验流程依序为,制程研发、临床试验,临床试验通过提出查验登记,接着量产、检验封缄后上市。但是在紧急授权(EUA)的情况下,因研发需要时间,为加速进行,各国在科学性前提下,采用不同方式简化行政流程。
陈时中说,为了加速紧急授权(EUA),研发阶段很多实验都是同步进行,为加速整体研发速度,若以流程ABC举例,一般流程依序为A、B、C,三者都需要通过,而在EUA情况下,研发到一个阶段后,就会开始同步进行下一部分,同样ABC三阶段都要通过才行。
采取紧急授权(EUA)的方式,会让厂商的财务风险增加,因需投资更多钱,陈时中进一步说明,每一阶段的实验都须要花很多经费,如果A还没做完,就展开B阶段,结果B做一半才发现A阶段失败,B阶段等于白做,事先投资的钱就浪费了,因为这样不是每个厂商都愿意这么做,因为实验没有保证成功。
各国也采取不同方式,分担厂商的财务风险,陈时中表示,以美国来说,会事先给药厂一大笔经费,要求加速研发,损失由国家吸收,又或者采取签约预采购的方式,政府预先支付20至40%不等的定金,签约金不再取回,实验失败就当作为政府投资,实验成功就进入下一步,各国也利用种种方法分摊厂商的财务风险,并加速疫苗研发。
也因为这样,政府也要求高端在EUA通过前,就先开始量产。陈时中说,若等到EUA通过才开始量产,等到实际有疫苗可用恐怕得等3个月至半年时间,也就失去公卫紧急效益,但万一EUA没过,政府就会支付材料费用,若通过EUA最好,疫苗就能及时上市。◇
责任编辑:郑桦